1. Unsur
Pengertian Unsur
Unsur merupakan zat tunggal yang tidak dapat dipisahkan lagi untuk menjadi zat-zat lain yang lebih sederhana dengan reaksi kimia biasa. Dalam kehidupan sehari-hari kita sangat mudah melihat dan mengenal unsur. Unsur suatu logam sangat mudah kita kenali dengan ciri-ciri permukaannya mengkilat, berbentuk padat kecuali unsur air raksa (Hg) yang memiliki bentuk cair.
Sebenarnya bumi yang kita pijak ini terdiri dari berbagai macam unsur. Berikut ini delapan jenis unsur yang membentuk hampir 99% bagian kerak bumi.
Tabel Unsur – Unsur Yang Membentuk Kulit Bumi
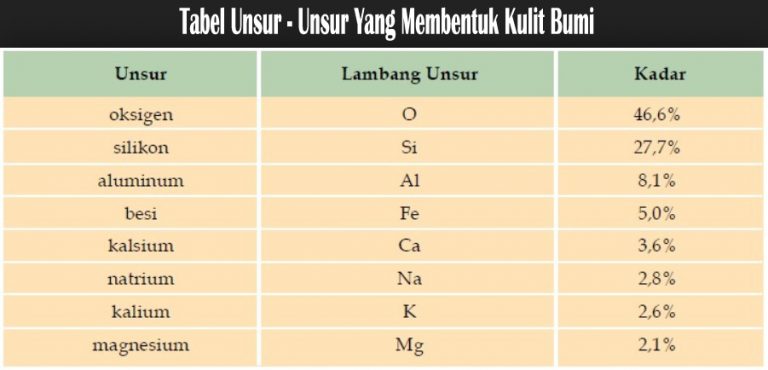
Unsur-unsur yang sudah dikenal ada yang berupa logam, bukan logam (nonlogam), dan semilogam. Logam adalah unsur yang memiliki sifat mengkilap dan umumnya merupakan penghantar listrik dan penghantar panas yang baik. Unsur-unsur logam umumnya berwujud padat pada suhu dan tekanan normal, kecuali raksa yang berwujud cair. Pada umumnya unsur logam dapat ditempa sehingga dapat dibentuk menjadi bendabenda lainnya. Beberapa unsur logam di antaranya besi, emas, perak, platina, dan tembaga. Contoh unsur-unsur logam ditunjukkan pada tabel berikut.
Tabel Unsur – Unsur Logam
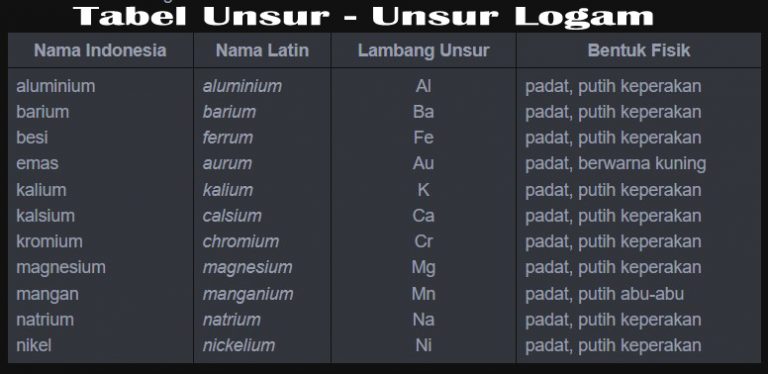
Adapun unsur nonlogam adalah unsur yang tidak memiliki sifat seperti logam. Pada umumnya, unsur-unsur nonlogam berwujud gas dan padat pada suhu dan tekanan normal. Contoh unsur nonlogam yang berwujud gas adalah oksigen, nitrogen, dan helium. Contoh unsur nonlogam yang berwujud padat adalah belerang, karbon, fosfor, dan iodin. Zat padat nonlogam biasanya keras dan getas. Unsur nonlogam yang berwujud cair adalah bromin. Perhatikan contoh unsur nonlogam pada tabel berikut.
Tabel Unsur – Unsur Nonlogam
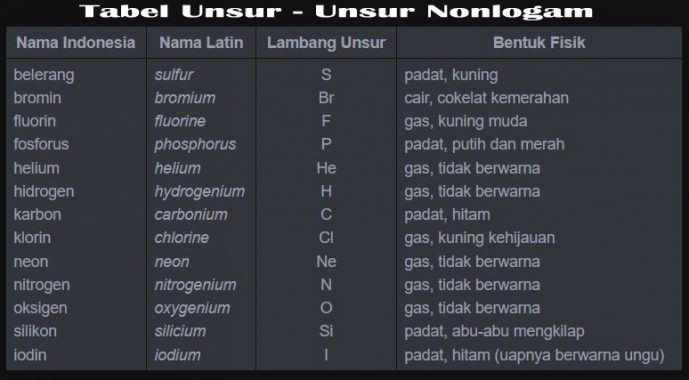
Selain unsur logam dan nonlogam ada juga unsur semilogam atau yang dikenal dengan nama metaloid. Metaloid adalah unsur yang memiliki sifat logam dan nonlogam. Contoh unsur-unsur jenis ini dapat kamu lihat padatabel berikut.
Tabel Unsur – Unsur Semilogam
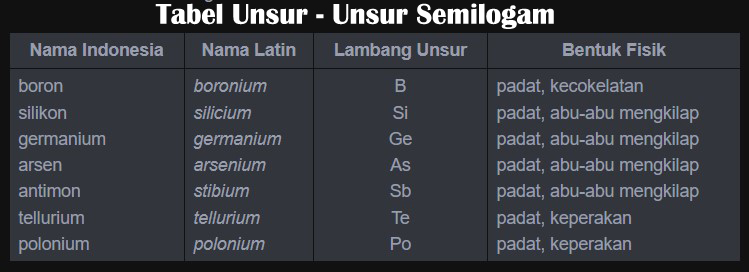
Unsur semilogam ini biasanya bersifat semikonduktor. Bahan yang bersifat semikonduktor tidak dapat menghantarkan listrik dengan baik pada suhu yang rendah, tetapi sifat hantaran listriknya menjadi lebih baik ketika suhunya lebih tinggi.
Di alam semesta ini terdapat 114 unsur baik alami maupun buatan. Unsur alami terdiri atas 91 jenis unsur dan 23 unsur sisanya merupakan unsur buatan.
Unsur-unsur tersebut dikelompokkan berdasarkan kemiripan sifatnya. Pengelompokan unsur ini dinamakan Tabel Periodik Unsur. Perhatikan Tabel Periodik Unsur pada gambar brikut.
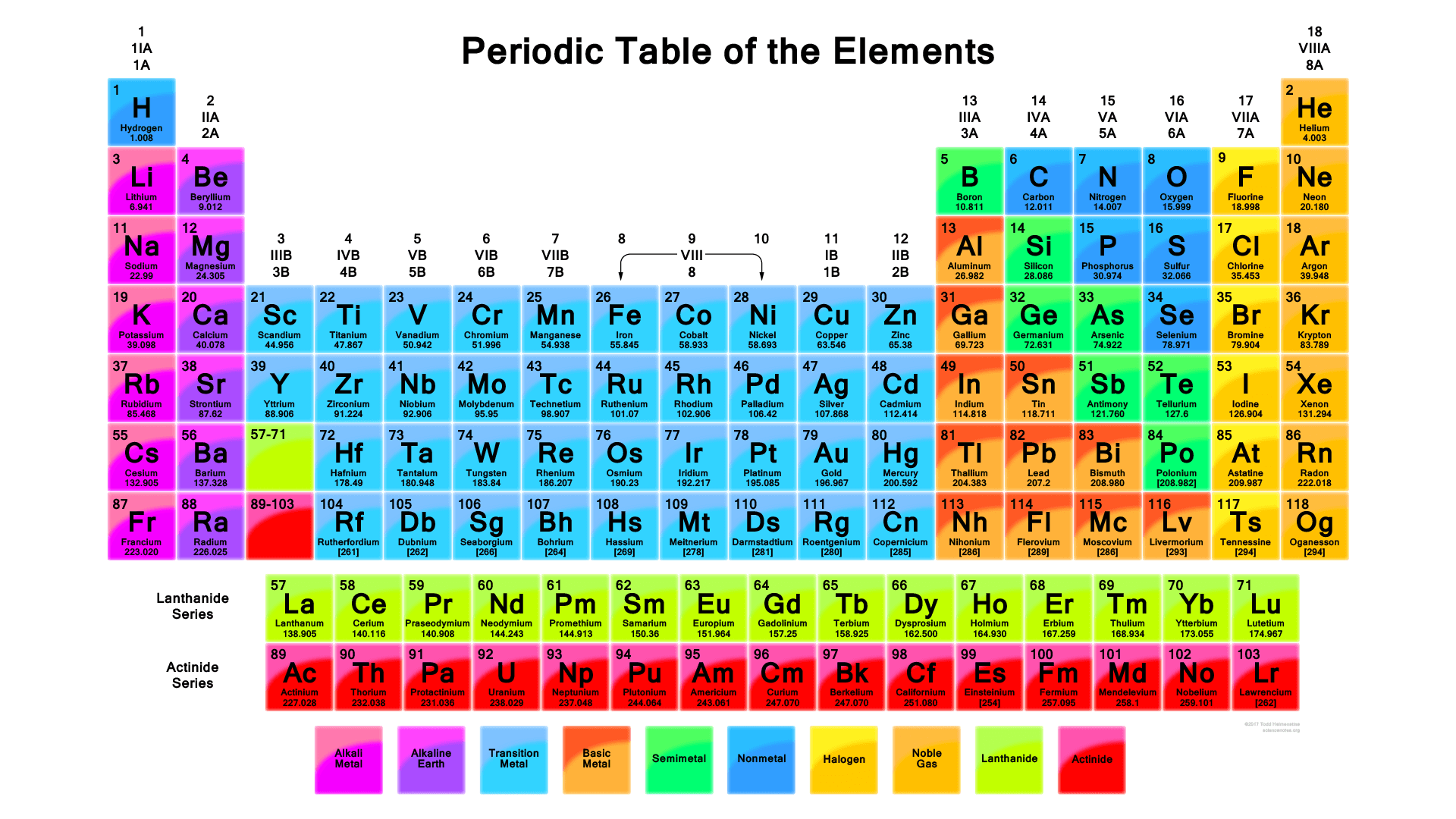
Sifat – Sifat Unsur
Sampai saat ini telah dikenal tidak kurang dari 114 macam unsur yang terdiri dari 92 unsur alam dan 22 unsur buatan. Berdasarkan sifatnya, unsur dapat digolongkan menjadi unsur logam, unsur nonlogam, serta unsur metaloid. Contoh unsur logam di antaranya besi, seng, dan tembaga. Contoh unsur nonlogam di antaranya karbon, nitrogen, dan oksigen. Silikon dan germanium tergolong metaloid.
Tabel Perbandingan Sifat Antara Unsur Logam Dan Nonlogam

2. Senyawa
Pengertian Senyawa
Senyawa merupakan zat tunggal yang masih dapat diuaraikan menjadi dua unsur atau lebih. Senyawa memiliki beberapa unsur yang saling bergabung secara kimiawi, sehingga lambang senyawa terdiri dari beberapa lambang unsur. Analisis untuk menemukan unsur-unsur penyusun suatu senyawa yang biasa disebut analisis kualitatif, sedangkan kalo analisis menemukan perbandingan setiap jumlah unsur dalam senyawa disebut analisis kuantitatif.
Senyawa Dapat di Kelompokan Menjadi Dua bagian Yaitu :
1. Senyawa Organik
Senyawa organik didifinisikan sebagai senyawa yang dibangun oleh suatu unsur karbon sebagai suatu kerangka utamanya. Senyawa-senyawa ini umumnya berasal dari makhluk hidup atau yang sering disebut organisme atau yang terbentuk oleh makhluk hidup.
Contoh Senyawa Organik :
- Ureum/Urea
- Gula pasir/sakarosa
2. Senyawa Anorganik
Senyawa anorganik adalah senyawa-senyawa yang tidak disusun dari suatu atom karbon, umumnya senyawa ini ditemukan dialam.
Contoh Senyawa Anorganik
- Asam Nitrat (HNO3)
- Natrium Klorida (NaCI)
- Almunium Hidroksida AI(OH)3
- Gas karbon dioksida (CO2)
Contoh lain Senyawa diantaranya yaitu:
- Asam Klorida (HCl)
- Air (H₂O)
- Asam Sulfat (H₂SO₄)
- Gas Hidrogen (H₂)
- Garam/ Natrium Klorida (NaCl)
- Gas Nitrogen (N₂)
- Gas Metana (CH₄)
- Gas Oksigen (O₂)
- Magnesium Klorida (MgCl)
- Amoniak (NH₃)
Sifat – Sifat Senyawa
Air merupakan contoh senyawa. Unsur-unsur pembentuk air adalah oksigen dan hidrogen. Jadi, air terdiri dari gas oksigen dan gas hidrogen yang bergabung melalui reaksi kimia. Air dengan rumus kimia H2O, memiliki sifat yang berbeda dengan unsur-unsur pembentuknya, yaitu H2 dan O2 yang berupa gas. Air dapat diuraikan menjadi unsur-unsur pembentuknya, sehingga disebut senyawa. Adapun hidrogen serta oksigen disebut unsur. Jadi, senyawa adalah zat yang terbentuk dari unsur-unsur dengan perbandingan tertentu dan tetap melalui reaksi kimia. Jadi, sifat senyawa tidak sama dengan sifat unsur pembentuknya. Senyawa dapat dipisahkan menjadi unsur-unsur atau menjadi senyawa yang lebih sederhana melalui reaksi kimia.
Di dalam tiap senyawa unsur-unsur penyusunnya mempunyai perbandingan massa yang tetap dan tertentu. Misalnya,
Di dalam tiap senyawa unsur-unsur penyusunnya mempunyai perbandingan massa yang tetap dan tertentu. Misalnya,
- Air (H2O), perbandingan massa unsur-unsur penyusunnya yaitu Hidrogen : Oksigen adalah 1 : 8
- Gula (C12 H22 O11), perbandingan massa unsur-unsur penyusunnya yaitu Karbon : Oksigen : Hidrogen adalah 72 : 88 : 11
- Etanol (C2 H5OH), perbandingan massa unsur-unsur penyusunnya yaitu Karbon : Oksigen : Hidrogen adalah 12 : 8 : 3
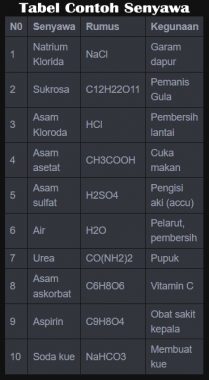
Beberapa contoh senyawa yang ada dalam kehidupan sehari-hari tercantum dalam tabel berikut.
Tabel Beberapa Contoh Senyawa dalam Kehidupan Sehari-hari
3. Campuran
Pengertian Campuran
Campuran merupakan materi-materi yang disusun oleh beberapa suatu zat tunggal baik berupa unsur atau senyawa dengan komposisi yang tidak tetap. Dalam campuran suatu sifat dari materi penyusunnya tidak bisa berubah karena gabungan beberapa zat tanpa melakukan reaksi kimia.
Campuran di Bedakan Menjadi Dua Yaitu Sebagai Berikut;
1. Campuran Homogen
Campuran homogen tersusun oleh dua bagian atau bisa lebih senyawa yang seluruh bagiannya memiliki sifat dan susunan lama. Larutan teridiri atas yang pertama pelarut (solvent) dan yang kedua zat terlarut (solute). Pada suatu campuran homogen seluruh bagiannya serbasama sehingga komponen-komponen penyusunnya tidak bisa dibedakan.
Contoh Campuran Homogen Yaitu :
- Larutan garam (Campuran garam dengan air)
- Larutan gula (campuran gula dengan air)
- Air aki (larutan asam sulfat)
- Cuka dapur
- Udara
- Alkohol 70%
2. Campuran Heterogen
Campuran Heterogen merupakan campuran serbaneka, dimana materi penyusunnya tidak berinteraksi, sehingga kita dapat mengamati dengan jelas dari materi penyusun campuran tersebut. Campuran heterogen tidak memerlukan kompisis yang tetap seperti halnya senyawa, jika kita mencampurkan dua materi atau lebih maka akan terjadi suatu campuran.
Contoh Campuran Heterogen
- Antara campuran minyak dan air, kita bisa melihat yang mana bagian minyak dan yang mana bagian air dengan indera matakita.
- Perhatikan pula susu yang sering kita konsumsi, terdiri dari atas berbagai macam zat seperti protein, karbohidrat, lemak, vitamin C dan E, dan mineral.
Sifat – Sifat Campuran
Suatu campuran dapat merupakan gabungan unsur dengan unsur, unsur dengan senyawa, atau senyawa dengan senyawa. Misalnya, stainless steel (baja tahan karat) terbuat dari campuran besi, krom, dan nikel. Komposisi unsur-unsur penyusun suatu campuran tidak tertentu, sehingga rumus kimia suatu campuran tidak dapat ditentukan. Pemisahan campuran dapat dilakukan secara fisika.
Tanah diklasifikasikan dalam campuran, yaitu campuran berbagai macam unsur dan senyawa. Sifat asli zat-zat pembentuk campuran masih tampak, sehingga komponen penyusun campuran tersebut dapat dikenali dan dapat dipisahkan lagi. Perbandingan zat-zat penyusunnya tidak tentu seperti pada senyawa.
Tabel Perbedaan Antara Senyawa dan Campuran

Semoga bermanfaat bagi pembaca. Sekian dan terimakasih.